Noţiuni fundamentale: sistem, stare, proces, echilibru.
Tag-uri
Partajeaza in Google Classroom

Transcript
în cea de a doua lecție de termodinamică
home introduce o serie de noțiuni
și mărimi de termodinamică 1 noțiune
de sistem stare și Ela grup termodinamic
sistemul termodinamic este un ansamblu
macroscopic de corpuri sau câmpuri
ce schimbă energie între ele Deci
interiorul sistemului sau cu exterior
starea termodinamică este un ansamblu
de parametrii Numiți parametrii
de stare și descriu complet un
sistem dermo dinamic La un moment
dat exemple de astfel de parametrii
sunt presiunea volumul temperatura
numărul de atomi sau molecule Deci
dacă specificăm valoarea Chester
parametri la un moment dat pentru
un sistem termodinamic atunci am
de scris starea termodinamică a
sistemului acel moment A5 parametrii
de stare sunt clasificați în funcție
de proprietățile lor în mai multe
grupe prima grupă conține noțiunile
de parametrii extensiv și intensiv
parametrii de stare sunt extensie
dacă cresc cu cantitatea de substanță
în un exemplu Evident fiind volumul
dar crește în cantitatea de substanță
din sistemul nostru Bineînțeles
că volumul va crește parametrii
se numesc intensiv dacă nu cresc
cu Cantitatea de substanță acest
tip de parametrii intensivi descriu
proprietățile locale ale sistemului
exemple fiind presiunea temperatura
densitatea și mod Evident în în
general putem avea presiunea între
anumit punct din sistem x y z și
presiunea poate lua o valoare local
bineînțeles ia poate fi și uniform
distribuită în sistem și atunci
valoarea presiunii este unică pentru
tot sistemul Dar în general ia
poate lua o valoare pentru un anumit
punct din sistem la fel și temperatura
sau densitatea pe când un parametru
extensiv precum volumul în nu poate
lua o valoare locală prin definiție
Nu are sens să vorbim de volumul
sistemului în punctul x y z Deci
prin definiție parametrii extensiv
sunt globali parametrii intensivi
sunt locali O altă clasificare
este următoarea parametrii de poziție
care descriu proprietățile spațiale
ale sistemului din nou volumul
fiind un exemplu evident și parametrii
de forță care descriu interacțiune
din sistem presiunea fiind un exemplu
ia de tracțiune din sistem dar
și temperatura Spre exemplu este
un parametru de forță echilibru
termodinamic al unui sistem are
loc atunci când toți parametrii
intensivi de stare rămân Constantin
Deci românii invariabil în timp
există două proprietăți importante
ale echilibrului termodinamic ale
stării de echilibru în prima fiindcă
am la echilibru toate sistemele
sunt omogene adică parametrii intensivi
care după cum am văzut sunt locali
de vin globali în sensul că de
vin uniforme valoarea lor este
uniformă în tot sistemul Deci din
nou stările de echilibru sunt și
stări omogene în care toți parametrii
intensivi sunt uniforme în sistem
de asemeni orice sistem termodinamic
dacă este lăsat să evolueze liber
adică nu intervenim din extinderea
exterior va evolua către o stare
de echilibru să vorbim acuma despre
noțiunea de proces termodinamic
procesul termodinamic este o transformare
de stare termodinamică În urma
interacțiunii cu mediul exterior
Deci starea termodinamică după
cum am văzut descrie sistemul la
un moment dat te și dacă intervenind
în exterior cu o interacție atunci
această stare termodinamică se
va modifica de naștere unui proces
Care este evoluția în timp a stărilor
termodinamice ale sistemului atât
starea finală cât și starea inițială
a unui proces în stări de echilibru
Ce corespund condițiilor externe
de dinainte și de după interacțiunea
cu mediul exterior stările intermediare
sunt totuși în general stări de
Nicky League dacă totuși procesul
e suficient de lemn încât aceste
stări intermediare să fi aproximate
cu stări de echilibru termodinamic
atunci procesul se numește Vasi
Static Deci din nou procesele în
cazul cel mai general au ca stări
de echilibru numai stalina inițiale
și finale cel intermediare fiind
de echilibru totuși în cazul particular
a proceselor foarte lente atunci
în fiecare etapă a procesului se
va obține un echilibru și în acest
caz procesul se numește cvasistatic
dacă procesul invers ce pleacă
din starea finală spre starea inițială
trece prin aceleași stări termodinamicii
intermediare procesul se numește
reversibil Deci schematic dacă
plecăm dintre o stare inițială
și mergem către o stare finală
pe un anumit drum și apoi facem
procesul invers plecăm din starea
finală spre starea inițială și
drumul se va întâmpla prin exact
acelea stări intermediare Atunci
cele două procese se numesc reversibile
în general nu este cazul când plecăm
din starea finală să spre starea
inițială putem lua alt drum adică
altă secvență de stări intermediare
caz în care procesul nu mai este
reversibil procesele cvasistatice
au proprietate importantă că pot
fi exprimate grafic prin diagrame
de evoluție un exemplu de astfel
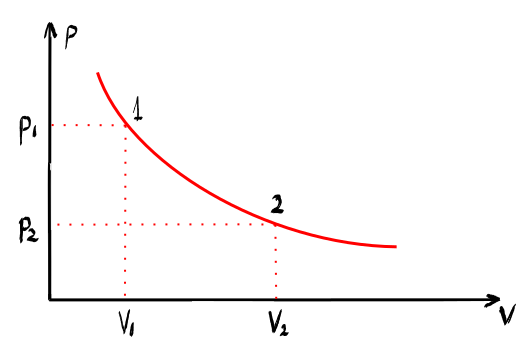
de diagramă de evoluție este așa
numita diagramă clapeyron în care
procesele sunt prezentate schematic
sau grafic în în sistem de coordonate
în care axa orizontală este volumul
ce are unitate de măsură metru
cub și cea verticală este presiunea
cu unitatea de măsură Pascal Deci
aceasta se numește o diagramă pe
V sau clapeyron și în care procesele
au anumită reprezentare grafică
fiecare punct de pe această de
pe această diagramă reprezintă
o stare Spre exemplu dacă luăm
un punct notat cu 1 aceasta va
fi starea unu a sistemului caracterizată
de presiunea P1 și V1 și volumul
V1 și așa mai departe starea 2
din nou foarte important de remarcat
în aceste diagrame de evoluție
este că pentru a putea avea o astfel
de reprezentare trebuie ca toate
punctele de pe diagramă să corespundă
unor stări de echilibru pentru
că altfel dacă o stare de pe diagramă
nu este o stare de echilibru atunci
nu putem defini o serie de parametri
precum presiunea sau temperatura
presiunea și temperatura stărilor
de echilibru nu pot fi definite
cel puțin nu în sensul clasic termodinamic
despre care vorbim acum de ce este
esențial ca procesele să fie casă
statice pentru a avea astfel de
diagrame de evoluție ultimul tip
de noțiune pe care îl introducem
este contactul sistemelor termodinamice
Dacă două sisteme termodinamice
se află inițial în echilibru termodinamic
și sunt puse în contact atunci
ele vor evolua spre un echilibru
în prin egalizare a parametrilor
intensivi dar anume acei parametrii
intensivi pe care contactul acest
contact dintre sisteme îi permite
Spre exemplu putem avea un așa
numit contact mecanic al ei două
sisteme termodinamice Spre exemplu
dacă avem două gaze separate de
un piston adiabatic și mobil adiabatică
înseamnă că nu permite schimbul
de căldură ești caldura nu este
permisă în acest context schimbul
de căldură Nu este permis Deci
mai exact avem o incintă separată
în două compartimente notate cu
a și b de un piston și acest piston
este mobil se poate mișca dar este
adiabatic asta înseamnă că nu permite
schimbul de căldură acest contact
se numește contact mecanic pentru
că permite egalizarea doar a parametrilor
intensiv de tip mecanic și anume
presiunea presiunea e legată de
forță Și de ce acest contact mecanic
va permite egalizarea presiunilor
celor două gazelor din cele două
din cele două compartimente un
alt exemplu de contact este contactul
termic contactul termic are loc
în cazul pistonului nostru dacă
el este diatermic adică permite
schimbul de căldură schimbul de
căldură are loc dar este fixat
Deci în acest caz avem aceeași
incintă separată de un piston în
două compartimente a și b Dar acest
piston este fixat și permite schimbul
de căldură Deci Acesta este un
contact termic de această dată
datorită proprietăților contactului
adică a pistonului parametrii intensivi
c se vor egaliza în cele două compartimente
între gazele din cele două compartimente
vor fi temperaturile de 5 final
temperatura gazului din compartimentul
a va fi egală cu cea din compartimentul
b concluzia un sistem două sisteme
aflate în contact vor tinde către
o stare de echilibru dar aceasta
are de echilibru va fi caracterizată
prin egalizarea parametrilor intensiv
pe care contactului permite nu
și a celorlalți