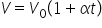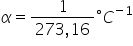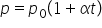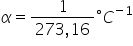Procese izobare. Procese izocore. Temperatura zero absolut.
Tag-uri
Partajeaza in Google Classroom

Transcript
În ciuda patra lecție de termodinamică
vom discuta despre procesele izobare
deschise de lege Gale suc și despre
procesele izocore descrise de legea
cea pentru studierea experimentala
procesul izobar folosim acest dispozitiv
experimental Ce conține o cuvă
în care se află apă și în interiorul
acestei cu Van Damme apă Care este
încălzită sau recită cu ajutorul
unui agent termic care circulă
prin această buclă Deci aceasta
este O buclă prin care circulă
un agent termic adică un lichid
cu temperatura fixă și variată
variată de către experimentator
iar temperatura apei este măsurată
cu ajutorul acestui termometru
deci de pe această scală vom citi
temperatura în interiorul cuvei
se află un balon Ce conține gazul
ale cărui proprietățile însă le
studiem și balonul se continuă
cu un tub inițial vertical și apoi
orizontal in care se afla o picătură
de mercur nici cu culoarea albastră
avem aici o picătură de mercur
Bineînțeles că această picătură
de mercur stabilește un așa numită
contact mecanic această noțiune
a fost discutată în cea de a doua
lecții de termodinamică practic
el se comportă ca un piston lăsat
piper și în concluzie se va mișca
în așa fel încât presiunea gazului
din interior să fie egală cu presiunea
atmosferică în concluzie obține
un așa numit proces izobar Adică
care are loc la presiune constantă
asta deoarece din nou presiunea
gazului va fi întotdeauna egală
cu presiunea atmosferică Care este
o constantă de procesul studiata
fii o dilatare izobară a gazului
din balon și în concluzie măsurăm
variația volumului Acest lucru
se face de pe această scală escală
tubul lui orizontal este calibrat
în așa fel încât să putem citi
de pe ea direct variația de volum
a gazului și Reprezentăm variația
reprezentând grafic variația de
volum a gazului în funcție de temperatură
a lui primul punct în măsurat primastar
a măsurat afine cea de la temperatura
de 0 grade si felul acesta se obține
următoarea lege simplă a variației
volumului gazului în funcție de
temperatura lui t și anume egal
cu 0 unde prin v0 înțelegem volumul
gazului la temperatura de 0 grade
Celsius înmulțită cu 1 plus Alfa
înmulțit cu temperatura Altfel
se numește coeficient de dilatare
izobară cel mai interesant lucru
pe care le observăm în legătură
cu acest coeficient este acela
că la schimbarea gaze gazului din
balon Alfa nu se schimba biciul
este independente gazul folosit
să discutăm un pic această lege
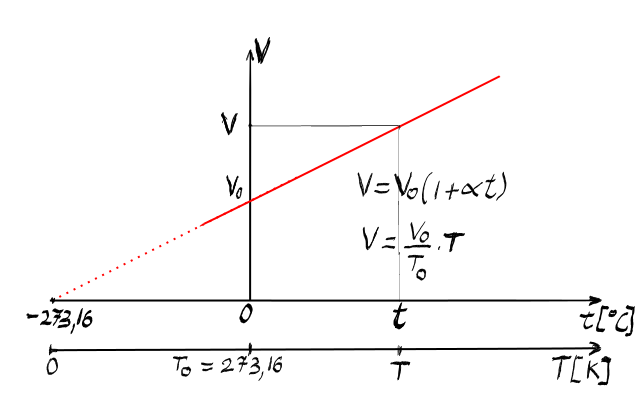
deci în primul rând să o reprezentând
grafic de centru o diagramă Vet
volume temperatură deci pe axa
verticală de volumul măsurat în
metri cubi pe orizontală temperatura
măsurată în grade Celsius obținem
o dependență liniară de genul acesta
unde primul punct cel de la 0 grade
Celsius are un volum v 0 iar apoi
la temperatura la temperatura finală
te avem un volum de aceasta este
reprezentarea grafică a datelor
experimentale pe care le obține
Ce este interesant de remarcat
după cum știm de Așa este că dacă
prelungim această dependență în
partea negativă axa de temperatură
ia o va intersecta la temperatura
absolută Deci punctul de intersecție
va fi la minus t 0 unde te 0 este
273 virgulă 16 grade Celsius în
această scală cer orizontală bine
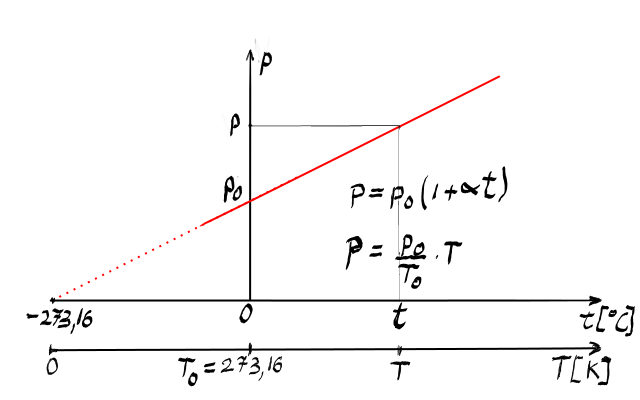
legea gay lussac pe care o scriu
din nou și anume vagal cu zero
înmulțit cu 1 plus alphaton obținem
Alfa coeficientul de dilatare izobară
este egal cu Delta V adică b minus
b 0 împărțit la 0 t Pe de altă
parte uitând ne pe acest grafic
și notând cu teta unghiul făcut
de dependența noastră de graficul
dependenței legii ale sec cu Axa
orizontală Deci graficul dependenței
liniare cu temperatura putem scrie
că tangentă reteta tangentă este
definită ca și cateta opusă împărțită
la cateta alăturată în triunghi
ce are un unghi de 90 de grade
ești unguent de teta poate fi scrisă
din acest triunghi ca fiind cateta
opusă adică Delta V această catetă
este vedea nu deci de asta e împărțită
la cateta alăturată unghiului Care
este temperatura taie Deci Delta
V împărțit la de asemeni același
aceeași tangenta unghiului teta
din acest triunghi poate fi scrisă
ca v0 cateta opusă este de 0 împărțit
la caseta alăturată teza Deci v
0 împărțit la 0 din această ecuație
putem scrii imediat că Delta V
împărțit la 0 este egal cu 1 pe
Tezeu combinând Cele Două ecuații
ecuații obținută din legea gay
lussac și cea din forma din geometria
dependenței volumului de temperatură
obținem imediat că coeficientul
de dilatare izobara Alfa este egal
cu unu pe trei zero Adică are valoarea
constantă de 1 pe la 273 virgulă
16 Kelvin la minus 1 acesta este
aceasta este motivul pentru care
acest cu eficientă este independent
de natură gazului folosit de asemeni
observăm imediat că dacă în loc
de o dependență a volumului de
temperatura Celsius transformăm
dependența întruna a volumului
de temperatura Kelvin această transformare
foarte simplă punctului minus testez
oră corespunde bineînțeles 0 Kelvin
prin definiție punctului zero ceea
ce corespunde 273 virgulă 16 Kelvin
și așa mai departe observăm că
volumul V ca funcție de temperatura
absolutum are o relație foarte
simplă și anume că z împărțit la
trei este constant deoarece este
o dependență liniară volumul împărțit
la temperatura absolută este o
constantă Aceasta este o a doua
forma legii gay lussac care spune
că pentru o masă de gaz constantă
aflată la presiune constantă din
nou aceasta deoarece procesul este
izobar volumul e proporțional cu
temperatura absolută să continuăm
cu studiul procesului izocor adică
un proces care are loc la volum
constant folosim același de dispozitiv
experimental ca în cazul studiului
procesului izobar și anume o cuvă
Care este umplută cu apă a cărei
temperatură este variată cu ajutorul
unui agent termic ce este circulat
prin acest drum și măsurăm temperatura
cu ajutorul termometrului de sticle
în interiorul cuvei avem un balon
în care se află un caz a cărei
proprietăți dorim să le studiem
apoi acest balon se continuă cu
un tub vertical și orizontal ca
înainte dar adăugăm un tub sub
formă de un vertical ca Ce conține
o coloană de mercur Bineînțeles
că atunci când vom crește temperatura
gazului cu ajutorul agentului termice
circulat în cuvin acesta se va
dilata o dată cu creșterea temperaturii
Noi dorim să avem un proces izocor
Deci trebuie să încercăm să obținem
un volum constant și facem acest
lucru primul următoarea tehnică
tubul sub formă de u are o bază
din cauciuc Deci porțiunea aceasta
a tubului este din cauciuc motiv
pentru din care și din acest motiv
putem să ridicăm sau să coborâm
partea din dreapta ramura din dreapta
tubului în clasa a opta ții învățat
că presiunea sau variația de presiune
indusă de o coloană de lichid este
egală cu densitatea lichidului
muncită cu accelerația gravitațională
și muncită cu înălțimea coloanei
de lichid în concluzie diferența
dintre volumul diferența de nivel
dintre coloana de mercur din stânga
și cea din dreapta va genera o
diferență de presiune Deci din
nou această diferență de nivel
generează o diferență de presiune
motiv pentru care Spre exemplu
dacă ridicăm ramura din dreapta
vom crește această presiune care
apoi va împinge gazul înapoi și
felul acesta avem o modalitate
de a menține volumul constant Deci
obținem un proces izocor în care
la fiecare măsurătoare a temperaturii
care duci ar duce la o variația
volumului obținem același volum
prin creșterea presiunii și mă
măsurăm aceste puncte experimentale
și anume variația de presiune Care
este dată de coloană de mercur
în ca funcție de temperatura în
de la deces primul punct sincer
la 0 grade c și obținem legea Charles
care spune că presiunea este egală
cu presiunea la omental 0 care
este și la temperatura 020 este
presiunea la 0 grade Celsius muncită
cu 1 plus b Tower temperatura Beta
este un coeficient numit coeficientul
termic al presiunii din nou schimbând
gazul din balon observăm că este
independent de gazul folosit acest
lucru este înțeles la fel ca pentru
procesul izobar Deci foarte rapid
reamintesc argumentație din acel
caz și anume dacă prezentăm reprezentând
grafic presiunea ca funcție de
temperatură obținem dependența
liniară din legea Charles și dacă
extrapolăm această dependență liniară
în partea negativă a temperaturii
obținem o intersecție cu Axa temperaturii
la o valoare minus 0 unde te zero
este zero absolut 273 virgulă 16
grade Kelvin exprimate exprimate
în acest caz de fapt în grade Celsius
pentru ca temperatura folosită
Este cea din scara C și din legea
si Elsa obținem că biata este egal
cu Delta pe împărțit la b 0 muzicute
iar din unde pe zero este presiunea
la 0 grade Celsius iar din forma
acestui grafic mai exact din valoarea
unghiului teta obținem la fel ca
în cazul procesului izo parcă tangent
de teta este egal cu Delta p supra
ten din acest triunghi Deci Delta
pe cateta aceasta împărțită la
temperatură iar din cel de al doilea
triunghi obținem că este egal cu
P 0 supra 3 0 pe 0 supra 3 0 deci
de aici obține încă deltapan împărțit
la pe zero este egal cu 1 supra
c 0 și luând în considerație ecuația
pentru Betta rezultă că Veta este
egal cu 1 pe 0 d c este egal cu
1 pe 273 virgulă si cand vin la
minus 1 aceasta fi motivul pentru
care acest parametru este independent
de natură gazului folosit în final
la fel dacă folosim în loc de o
axă a temperaturii în grade Celsius
una absolută în grade Kelvin obținem
că presiunea împărțită la temperatură
este o constantă mai exact este
tangentă de tata ca tangenta este
pe supra absolut Deci legea Charles
se poate formula în felul următor
pentru o masă de gaz constantă
aflată la volum constant ceea ce
înseamnă proces izocor presiune
proporțională cu temperatura absolută
să încheiem cu câteva considerații
în legătură cu temperatura zero
absolut Kelvin a stabilit următoarele
lucruri expirăm toate procesele
export izobare în care se reprezintă
volumul ca funcție de temperatură
pentru toate gazele folosite sunt
extrapolate la un volum zero în
acest punct 0 egal cu minus 273
virgulă 15 grade De ce a făcut
Kelvin a repetat pentru multe gaze
acest tip de experiment volumul
ca funcție temperatură la presiune
constantă și a obținut varii dependențe
liniare dar toate extrapolând dusei
în același punct minus teze unde
te 0 are această valoare apoi a
repetat un experiment de tip izocor
adică la volum egal constant și
a reprezentat presiunea ca funcție
de temperatură obținând iarăși
dependențe liniare dar care extrapolate
duceau pentru toate cazurile toate
gazele Spre exemplu la același
punct teze de aici Ia tras concluzia
foarte importantă că există o temperatură
minimă universală universală Adică
care se obține în toate procesele
termodinamice pentru toate tipurile
de gaze ce nu poate fi atinsă prin
și un proces adică putem doar extrapola
ne putem apropia numai asimptotic
de această valoare Dar nu poate
nu o putem atinge în experimente
niciodată această temperatură sau
numit temperatura de absolut Care
este folosită în Cara absolut sus
Caracal