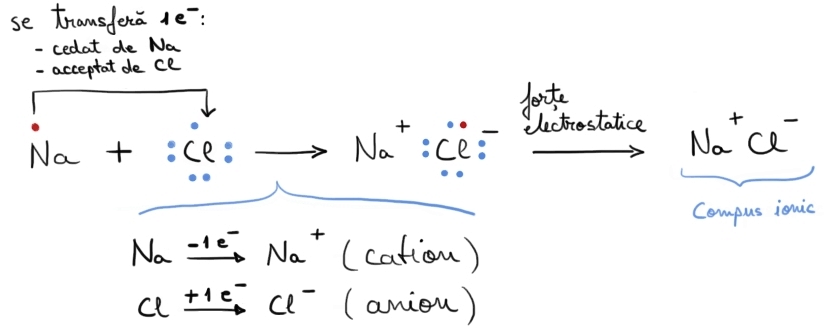
Legătura ionică. Compuşii ionici.
Partajeaza in Google Classroom

Transcript
Până acum am vorbit despre atomi
individuali despre elemente și
despre proprietățile lor atomii
sunt particulele fundamentale ale
materiei însă dacă ar exista în
natură numai sub această formă
de atomi nimic din ceea ce ne înconjoară
nu ar mai exista diversitatea imensă
de compuși naturali sau sintetizați
de noi în laborator pe care îi
formează elementele chimice se
explică prin tendința generală
a atomilor de ajunge într o stare
de energie minimă această stare
de energie minimă înseamnă preferință
spre a depune cât mai puțin efort
sau energie pentru a exista între
stare cât mai stabilă adică un
fel de stare de confort ridicat
la acel mai mic os posibil În cazul
atomilor asta presupune realizarea
unei structuri electronice stabile
pe ultimul strat de structuri electronice
stabile corespunzătoare gazului
inert celui mai apropiat din tabelul
periodic știind că gazele inerte
au configurația de octet pe stratul
exterior cu excepția heliului care
are configurație de duble configurații
care le oferă acestor gaze inerție
chimică astfel a luat naștere o
regulă și anume regula octetului
care spune că de cele mai multe
ori configurația stabilă la care
ajung atomii este de 8 electroni
pe ultimul strat există trei modalități
prin care atomi elementelor pot
ajunge la astfel de configurații
stabile prin cedare de electroni
prin primire de electroni sau prin
punere în comun de electroni în
reacții cu alții atomi când se
formează Legături chimice putem
spune că legătura chimică e o pereche
de electroni împărțită de doi atomi
iar această pereche de electroni
acționează ca o forță ce ține atomi
împreună și face să acționeze ca
o moleculă independentă dar tipul
legăturii chimice depinde de felul
în care aceștia Tomi împart perechea
de electroni între ei Deci dacă
vorbim despre transfer de electroni
de la un atom la altul adică un
atom cedează și altul primește
când rezultă Ioni între care se
exercită forțe de atracție electrostatică
înseamnă că vorbim despre legături
ionice când atomii impun în comun
electroni Deci punere în comun
de electroni atunci e vorba despre
legături Valente în cazul metalelor
în stare elementară între atomi
se stabilește un tip special de
legătură care se numește legătură
metalică și care ține tot de un
fel de punere în comun de electroni
să începem cu legătura Ionică pentru
a înțelege mai bine ne vom referi
bineînțeles și la compuși ionici
după cum am zis să o metoda de
a atomilor de ajunge la configurația
stabilă este de a ceda electroni
devenind astfel Ion pozitivi Sau
de a primi electroni devenind astfel
Ion negativi electronul Sau electronii
care se plimbă în acest fel de
la un atom la altul sunt particule
foarte reactive A nu pot exista
liber de capul lor natură Deci
în vecinătatea unui atom care cedează
electroni se află întotdeauna un
atom care acceptă electroni vom
lua exemplu sodiului și al clorului
știind că elementele din grupele
unu și doi sau unul principal și
a doua principală și donează electronii
de valență fără prea multe probleme
sunt foarte generoși a se transformă
azi fel în Ioni pozitivi sau cati
ani Deci sodiul din grupa 1 cu
numărul Atomic Z egal cu 11 are
această configurație 1 S2 2 S2
2p 6 3S 1 de aici până aici este
configurația gazului rar care se
află înaintea sodiului în tabelul
periodic adică a neonului și la
care sodiul își dorește foarte
tare să ajungă Deci va ceda aceste
tron și după cum știm configurația
sodiului se mai poate scrie și
în acest fel configurația neonului
și trei S1 sodiul va scăpa de electronul
care îl incomodează iar configurația
lui va fi doar configurația neonului
și vedem că solul sa transformat
în drum Ioan pozitiv Pe de altă
parte atomii elementelor din grupele
16 și 17 sau a 6-a principală și
a șaptea principală preferă să
primească electroni pentru a ajunge
la configurația gazului nobil imediat
următor în perioada astfel se transformă
în Ioni negativi sau anioni cum
se întâmplă cu clorul de exemplu
el vrea să ajungă la configurația
gazului nobil argon configurația
clorului care are numărul atomic
Z egal cu 17 neon trez 2 3 pe 5
electronul de la sodiu va fi acceptat
de clor care devine astfel una
Ion negativ cu următoarea configurație
neon 3 s 2 3 pe 6 această configurație
fiind echivalentă cu configurația
argonului Haideți să desenăm electronii
de valență ca fiind niște puncte
în jurul atomilor Acestea fiind
simboluri Lewis sodiul are un electroni
de valență deci îi desenăm un punct
iar clorul are șapte electroni
de valență Deci vom desenat șapte
puncte două aici două și încă două
și unul procesele care au loc pot
fi reprezentate în modul următor
un electroni transferat de la sodiu
la clor sodiul devine un cation
iar clorul un onion ce are configurație
de octet acum sunt amândoi atomi
foarte fericiți cu structurile
lor stabile de pe ultimul strat
numai că sunt atrași unul de altul
Cei doi Ioni de semn contrar se
atrag prin forțe de natură electrostatică
aceste forțele electrostatice Se
supun legii lui Columb dar putea
să știți de Columb de la fizică
car lege care pe scurt zice că
sarcinile de același semn se resping
iar sacele de semne opuse Piatra
UGG de atracție electrostatică
dintre sarcină pozitivă a sodiului
și cea negativă a clorului este
asimilată cu o legătură chimică
numită legătură Ionică sa format
astfel un compus chimic nou format
din Ion și care se numește compus
ionic clorura de sodiu obținută
astfel este de fapt sarea de bucătărie
după cum bine știți ea a solidă
b chiar cristalină în cele mai
multe dintre substanțele solide
fiecare particulă Ionatan sau moleculă
ocupă o anumită poziție între un
aranjament ordonat exact ca în
această imagine adică se formează
o rețea cristalină astfel de substanțe
se numesc substanțe cristaline
De ce acest ansamblu geometrii
regulat format din Ioni de sodiu
plus și clor minus se numește rețea
Ionică dacă vă mai amintiți Ionela
gătit sunt mai voluminoși datorită
electronilor în plus deci ionii
de clor sunt aceștia clor minus
clor minus iar cei pozitivi au
un volum mai mic Deci Ioni de sodiu
sunt aceștia sodiu plus sodiu plus
data viitoare Că un vas condimentat
cu sare cartofi prăjiți sau Ciorba
gândiți văd că intru în singur
cristal de sare se află de fapt
un număr mai mare de Ion decât
numărul de stele existente în tot
universul Vizi Așadar legătura
Ionică se realizează pe baza transferului
de electroni de la atomii elementelor
cu caracter metalic la atomii elementelor
cu caracter nemetalic și pe baza
ei interacțiuni electrostatice
între ionii Formați legăturile
ionice se întâlnesc în săruri precum
clorura de argint ionii sunt argint
plus și flori minus în clorura
de sodiu despre care am vorbit
tu Ioni sodiu plus și clor minus
sau sulfatul de cupru cu Ioni cupru
2 plus și Gruparea Sulfat 2 minus
legăturile ionice se mai întâlnesc
și în unii oxizi bazici Cum sunt
oxizii metalelor alcaline e precum
oxidul de sodiu cu Ioni sodiu plus
și oxigen 2 minus sau în oxizii
metalelor alcaline o pământ oase
precum oxidul de calciu calciu
2 plus și oxigen 2 și majoritatea
hidroxizilor au tot legături ionice
de exemplu hidroxidul de sodiu
sau hidroxidul de magneziu avem
Ioni sodiu plus și grupare hidroxil
minus la fel magneziu 2 plus și
Gruparea hidroxil minus despre
legătura Ionică mai e foarte important
de reținut faptul că nu este orientată
în spațiu Deci nu are orientare
în spațiu adică nu formează molecule
Forțele de atracție electrostatică
acționează în toate direcțiile
formând acea rețea cristalină adică
compușii ionici pentru ca aceste
forțe care se exercită între Ion
sunt foarte puternice compuși ionici
sunt substanțe solidă cu puncte
de topire și fierbere ridicate
compușii ionici solubile în apă
formează soluții care conduc curentul
electric despre legătura Ionică
și compușii ionici urmează să vorbim
și despre legătura covalentă și
despre compușii moleculari