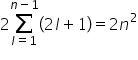Principiul de excluziune Pauli. Straturile şi substraturile electronice.
Tag-uri
Partajeaza in Google Classroom

Transcript
în cea de 10 lecții de fizică atomică
în fond continua discuția din lecția
precedentă despre atomul cu mai
mulți electroni în care am introdus
modelul de pături al atomului bazat
pe cele patru numere cuantice n
l m și MS Haideți să vedem cum
anume este folosit acest model
al pădurilor electronice în stabilirea
structurii Și Proprietăților atomilor
se pleacă de la un principiu foarte
important numit principiul de excluziune
Pauli spune foarte simplu că întrun
atom sau o moleculă sistem Atomic
fiecare electroni caracterizat
de un set de numere cuantice aceste
patru numere cuantice care le am
de scris ce diferă de cel al cărui
alt electroni acest sistem altfel
spus nu există doi electroni în
același atom care să aibă același
sens acest set de numere este unic
pentru un electron dat odată ce
alege un alt electroni atunci cel
puțin unul din aceste numere trebuie
să fie diferit setul de numere
cuantice e unic pentru electronul
da și atunci putem faci următoarea
clasificare și după ce introducem
această clasificare a stărilor
electronice vom folosi principiul
de excluziune Pauli pentru a vedea
Ce consecințe are asupra proprietăților
atomi se numește pătură sau strat
elektronic ansamblurilor din turn
atom cu același număr cuantic principal
an în continuare cel mai important
număr cuantic rămâne and Cașin
atomul Bor pentru că e el descrie
energia după ca ma sus nu în totalitate
dar în cea mai mare parte și în
concluzie energia fiind cea mai
importantă caracteristică a unui
electron principala categorisire
sau clasificare a electronilor
este după acest număr cu anti principal
n și cei care au același an formează
păturile electronice se folosesc
următoarele simboluri de ceea ce
acestea sunt Notați toți electronii
care au n egal cu 1 vor forma pătura
ca cei cu An egal cu doi vor forma
pătura el și așa mai departe an
egal cu 3 pe 3 m de ce acestea
sunt notațiile păturilor electronice
Haideți să scriem încă o dată explicit
Care sunt valorile acestor numere
cuantice Deci după cum am văzut
n ia orice valoare scuzați nu de
la zero și de la 1 1 2 3 și așa
mai departe Deci un număr infinit
de Valori pentru in avem pentru
el am văzut că le ia orice valori
între 0 inclusiv și m minus 1 inclusiv
Deci avem n valori a lui el apoi
pentru m am văzut că avem orice
valori între minus el inclusiv
și plus el inclusiv De ce există
2 L plus 1 valori ale lui m iar
m s am văzut că ia două valori
și anume plus minus 1 pe 2 deci
MS are două valori De ce este important
să cunoaștem aceste numere de valori
ale numerelor cuantice esti este
faptul că putem calcula numărul
de stări în particular Spre exemplu
numărul de stări dintre o pătură
care va fi numărul maxim de electroni
de pe acea pătură este 2 m La pătrat
de ce Pentru că pur și simplu o
pătură este Ansamblul de electroni
cu acum am dat da Și deci dacă
n este dat putem calcula Câte valori
Câte sat Câte seturi de numere
cuantice putem avea pentru m fixat
să spunem că n este egal cu 3 adică
ne aflăm pe pătură Câte stări posibile
Deci Câți electroni putem avea
maxim pe un o pătură m și atunci
avem n valori pentru el Deci sumă
el de la zero la el minus unu iar
pentru Ema avem 2 L plus 1 Deci
2 L plus 1 valoarea lui m înmulțit
asumat de la el egal cu 0 la A
minus 1 și înmulțit cu 2 pentru
m dacă facem acest calcul vedem
că o pătură poate avea maxim 2
m pătrat electronic Spre exemplu
pe om poate avea maxim 18 electroni
datorită acestui principiu de excluziune
se numește substrat electronic
ansamblul electronilor cu același
număr cu anticor Beetle el Deci
odată ce am stat Am fixat inul
și am fixat Deci pătura Pentru
a stabili structura păturii sau
stratului mergem la substanță dacă
vreți sub pătură iar aceasta va
fi definită de următorul număr
cuantica importanță și anume el
simbolurile pentru substraturi
sunt s p d e f și g care corespund
lui valorilor lui l egal cu 0 1
2 3 4 și așa mai departe și bineînțeles
numărul maxim de electroni pe un
substrat este 2 ori 2 L plus unu
pentru că o dată ce am fixat an
și el Deci am fixat pătura sau
straturi și substraturi de cm și
el sunt fix atunci nu mai m și
m s pot varia și numărul posibil
maxim de valori ale combinației
MMS va fi de 2 ori 2 L plus 1 bun
Haideți sunt stabilim acum structura
atomilor în principiu ocuparea
substraturilor cu electroni se
face conform principiului lui Pauli
și a principiului minimei energii
deci ar trebui să avem următoarea
structură Ce Ce înseamnă Ce înseamnă
acest lucru Păi dacă luăm n egal
cu unu care înseamnă o pătură de
tip k după cum am văzut pentru
n egal cu 1 s l poate lua valorile
de la zero la emisiuni deci el
poate lua numai valoarea 0 asta
implică că pătura ca are următoarea
structură posibilă 1 s Adică n
egal cu 1 l egal cu 0 aceasta sunt
singur le valori posibile ale combinației
an el într o pătură ca Haideți
să luăm n următoarea n egal cu
2 Scuzați n egal cu 2 ce implică
după ca ma sus o pătură el El atunci
poate a luat valorile de la 0 la
n minus unu deci de la 0 la 1 Avem
două valori posibile ale lui el
asta implică că pătura el are următoarea
structură 2s 2p nici combinațiile
n l sunt doi zero doi unu adică
2s 2p Deci pătura ca este aceasta
pătura El este aceasta mai departe
încă una n egal cu 3 care este
pătura m pentru n egal cu 3 l ia
valorile 0 1 și 2 asta implică
că pătura m este formată din stările
3S 3p și 3D Deci aceasta va fi
structura maximă posibilă a pădurii
m și aceasta este pătura m ordinea
lor este bineînțeles dată de principiul
minimei energii o pătură are un
an fixat Deci Pe măsură ce crește
A nu crește energia totuși în practică
datorită faptului că energia electronilor
depinde și de momentul cinetic
orbital Deci energia acestor stări
depinde și de el Nu Numai de m
ocuparea substraturilor cu electroni
se modifică un pic din nou această
ordonare este cea a energiilor
aceste stări au energia crescătoare
dar deoarece energia depinde și
de valoarea lui el adică spdf nu
numai de valoarea lui n avem în
practică următoarea ordonare Deci
primele cinci stări rămân aceleași
dar între 3D și 4s apare o inversare
în principiu 3D are n mai mic decât
4s bineînțeles n egal cu 3 n egal
cu 4 Deci în principiu dacă energia
depinde numai de m3de ar trebui
să fie în fața lui 4s dar deoarece
există o mică componentă ce depinde
de el a energiei în realitate 4s
are energie mai mică decât 3D și
la fel apoi obținem veri alte inversări
Deci în realitate calcule teoretice
și măsurătorile experimentale dau
această ordine a stărilor electronice
ținând cont de această schemă După
aceea putem foarte ușor stabili
structura atomilor hidrogenul care
are Zet egal cu 1 Deci un electroni
îl va avea cel un electroni pe
starea unui esti heliu care are
Zet egal cu doi de doi electroni
va avea ci doi electroni pe stat
pe starea unui s comentariu fiecare
din aceste stări poate avea maxim
doi electroni Ce corespund lui
m este egal cu plus minus 1 pe
2 Deci cei doi electroni de pe
1 s vor fi vor corespunde lui unul
lui m s egal cu plus 1 pe 2 celălalt
lui m este egal cu minus 1 pe 2
și așa mai departe litiu care are
Zet egal cu 3 va avea doi electroni
pe 1s de al treilea electron nu
mai îmi poate pune pe unul este
de ce am spus unul s are numai
două stări Deci trebuie să meargă
la următorul la 2s și pune un electroni
al treilea electrom pe dos beriliu
următorul atomi din tabel Mendeleev
va avea patru electroni Deci va
umple atât 1s cât și 2s borul care
vine cu al cincelea electron trebuie
să treacă cu el pe 2p carbonul
cu Zet egal cu 6 Completează 2
pe el urmând ca azotul cu Z egal
cu 7 să trebuiască să treacă cu
cel de șaptelea electron Petre
s și ultimul exemplu care îl dăm
oxigenul cu Z egal cu 8 Completează
3 și așa mai departe în concluzie
combinația dintre principiul excluziunea
lui Pauli și calcule exacte ale
energiei acestor stări cuplate
cu principiul min energiei duce
la faimosul tabel Mendeleev deci
putem înțelege foarte ușor pe baza
acestor considerații clasificarea
atomilor din tabelul lui Mendeleev
proprietățile lor chimice de bază
precum numărul de electroni de
valență periodicitatea proprietăților
atomilor din tabelul Mendeleev
și așa mai departe plecând de la
aceste principii