Aminoacizi
Tag-uri
Partajeaza in Google Classroom
Teorie: Teorie - Aminoacizi Descarcă PDF
În organismele vii, proteinele au o varietate imensă de structuri şi funcţii. În toate organismele vii, fie că e vorba de bacterii, sau de organismul uman, proteinele sunt formate din aceeiaşi 20 de aminoacizi naturali.
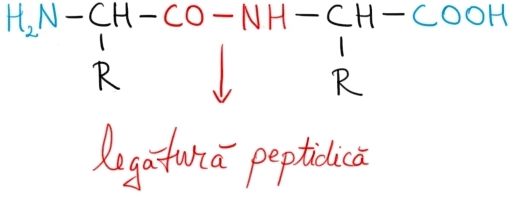
Proteinele sunt polimeri ai aminoacizilor, polimeri formaţi prin reacţii complexe de policondensare. Fiecare rest de amnoacid din structura unei proteine este legat de vecinul său printr-o legătură covalentă specifică numită legătură peptidică. Legătura peptidică dintre doi aminoacizi este reprezentată în imaginea de mai jos:
Caracteristici structurale comune ale aminoacizilor naturali: toţi cei 20 de aminoacizi sunt α–aminoacizi, şi au o grupă funcţională carboxil (– COOH) şi o grupă funcţională amino (– NH2) legate de acelaşi atom de carbon, şi anume atomul de carbon din poziţia α, Cα. Poziţia α este poziţia vecină grupei carboxil.
Caracteristici structurale diferite ale aminoacizilor naturali: aminoacizii diferă între ei prin catenele lor laterale, adică prin radicalii hidrocarbonaţi, notaţi generic cu R. Aceşti radicali hidrocarbonaţi au structuri, dimensiuni şi sarcini electrice variate, şi influenţează solubilitatea în apă a fiecărui aminoacid în parte.
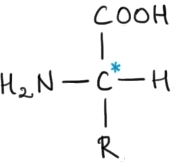
Atomul de carbon din poziţia α este legat de 4 grupuri diferite de atomi, ceea ce-l face un atom de carbon asimetric, sau un centru de chiralitate. Aceste 4 grupuri diferite de atomi sunt grupa carboxil, grupa amino, radicalul hidrocarbonat şi un atom de hidrogen. Excepţie face glicina care are un atom de hidrogen în locul radicalului hidrocarbonat. Imaginea de mai jos prezintă structura generală a unui α–aminoacid:
Configuraţiile zaharurilor simple şi ale aminoacizilor sunt specificate prin sistemul D,L.
Aminoacizii naturali (cu excepţia glicinei) pot exista sub forma a doi enantiomeri D şi L:
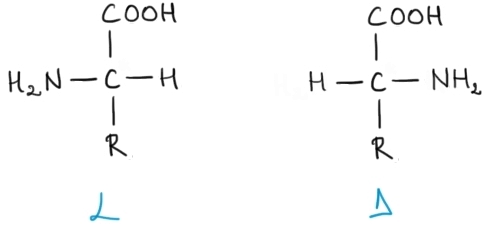
Prin convenţie, s-a decis că α–aminoacizii naturali fac parte din seria sterică L, iar enantiomerii lor din seria D. Enantiomerii L se reprezintă întotdeauna cu grupa amino în partea stângă şi cu atomul de hidrogen în partea dreaptă.
Resturile de aminoacizi din proteine se găsesc, exclusiv, sub formă de stereoizomeri L.
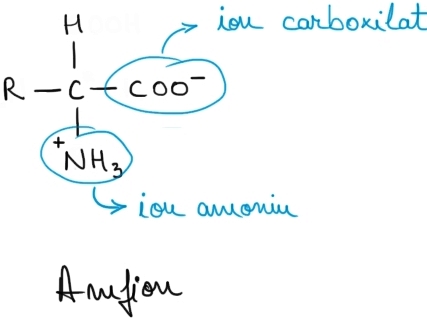
Coexistenţa celor două grupe funcţionale în structura aminoacizilor determină o ionizare intramoleculară prin care aminoacizii se transformă în amfioni, adică în ioni care conţin atât o sarcină negativă, cât şi o sarcină pozitivă. Imaginea de mai jos prezintă un aminoacid sub forma lui de amfion:
Aminoacizii naturali pot fi clasificaţi în funcţie de structura şi proprietăţile catenelor laterale hidrocarbonate. Astfel, avem următoarele clase de aminoacizi:
- Aminoacizi cu radicali nepolari, alifatici: alanina, valina, leucina, izoleucina, glicina, prolina, metionina.
- Aminoacizi cu radicali aromatici: fenilalanina, tirozina, triptofanul.
- Aminoacizi cu radicali polari, fără sarcină electrică: serina, treonina, cisteina, asparagina, glutamina.
- Aminoacizi cu radicali cu sarcină pozitivă (caracter bazic): lisina, arginina, histidina.
- Aminoacizi cu radicali cu sarcină negativă (caracter acid): acidul aspartic, acidul glutamic.
Datorită caracterului dipolar, de amfion, aminoacizii pot reacţiona atât ca acizi, cât şi ca baze. Aşadar, aminoacizii au caracter amfoter.
Soluţiile tampon sunt soluţii care nu îşi modifică seminificativ pH-ul la adăugarea unei cantităţi mici de acid tare sau de bază tare.
Soluţiile apoase de aminoacizi sunt soluţii tampon.






