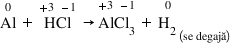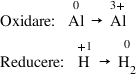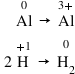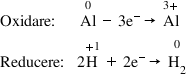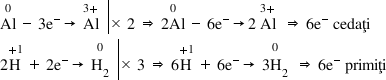Stoechiometria se referă la calculul cantităţilor relative de reactanţi şi produşi care iau parte la o reacţie chimică.
Coeficienţii stoechiometrici arată numărul de molecule de reactant care participă la reacţie, şi numărul de molecule de produs care se formează. Cu alte cuvinte, coeficienţii stoechiometrici arată relaţiile cantitative dintre participanţii la o reacţie chimică. Pentru o ecuaţie chimică generală de forma celei de mai jos, a, b, c, şi d sunt coeficienţii stoechiometrici corespunzători reactanţilor A şi B, respectiv produşilor C şi D.
aA + bB 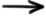 cC + dD
cC + dD
Analiza proceselor de oxidare şi de reducere care au loc în timpul unei reacţii este foarte utilă pentru stabilirea coeficienţilor stoechiometrici ai reacţiei respective. Această metodă de stabilire a coeficienţilor stoechiometrici se numeşte metoda redox şi se bazează pe faptul că, într-o reacţie redox, numărul electronilor primiţi trebuie să fie egal cu numărul electronilor cedaţi.
Metoda redox aplicată pe reacţia dintre aluminiu şi acidul clorhidric:
Al + HCl 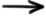 AlCl3 + H2
AlCl3 + H2
Etape pentru stabilirea coeficienţilor stoechiometrici:
1. Se stabilesc numerele de oxidare ale tuturor atomilor, identificându-se atomii care îşi modifică numărul de oxidare:
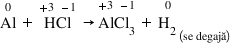
2. Se scriu ecuaţiile celor două semireacţii, de oxidare şi de reducere:
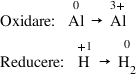
3. Se egalează numărul de atomi din fiecare semireacţie:
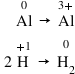
4. Se stabileşte numărul de electroni primiţi sau cedaţi în fiecare semireacţie:
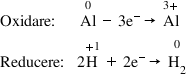
5. Se echilibrează cele două semireacţii ţinând cont că numărul de electroni cedaţi trebuie să fie egal cu numărul de electroni primiţi. Pentru acest lucru trebuie să se găsească cel mi mic multiplu comun al numerelor de electroni transferaţi între cele două semireacţii.
În acest caz, cel mai mic multiplu comun este 6. Împărţim această valoare la numărul electronilor cedaţi (în procesul de oxidare), iar cu valoarea obţinută înmulţim semireacţia de oxidare, obţinând astfel coeficienţii stoechiometrici pentru aluminiu şi pentru clorura de aluminiu. La fel se procedează şi cu semireacţia de reducere, obţinând astfel coeficienţii stoechiometrici pentru acidul clorhidric şi pentru hidrogen
.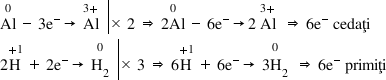
6. Se introduc coeficienţii astfel obţinuţi în ecuaţia globală a reacţiei:
2Al + 6HCl 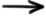 2AlCl3 + 3H2
2AlCl3 + 3H2
7. Dacă este cazul, se stabilesc şi coeficienţii celorlalte specii chimice care iau parte la reacţie.

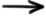 cC + dD
cC + dD