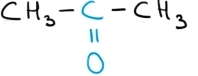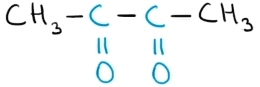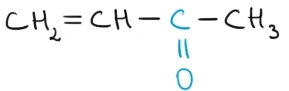Compuşii carbonilici
Tag-uri
Partajeaza in Google Classroom
Teorie: Compuşii carbonilici Descarcă PDF
Grupa funcţională carbonil este reprezentată de un atom de oxigen legat de un atom de carbon printr-o legătură dublă: C = O.
Compuşii carbonilici sunt compuşii organici care conţin grupa funcţională carbonil.
Aldehidele sunt compuşii carbonilici în care grupa carbonil este legată de un radical organic R, şi de un atom de hidrogen:
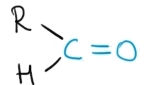
Cetonele sunt compuşii carbonilici în care grupa carbonil este legată de doi radicali organici R, identici sau diferiţi:
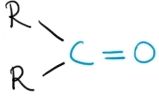
Formaldehida este primul termen din clasa aldehidelor şi, este o excepţie, întrucât atomul de carbon din gruparea carbonil se leagă de doi atomi de hidrogen: H2C = O.
Compuşii carbonilici au structuri foarte diverse. În funcţie de natura grupei carbonil, compuşii carbonilici pot fi aldehide sau cetone. În funcţie de natura radicalilor hidrocarbonaţi, compuşii carbonilici pot fi saturaţi, nesaturaţi sau aromatici. De asemenea, compuşii carbonilici mai pot fi compuşi monocarbonilici sau compuşi policarbonilici, în funcţie de numărul grupelor carbonil prezente în moleculă.
Denumirea aldehidelor: o metodă de denumire a aldehidelor este prin adăugarea sufixului –al la numele hidrocarburii cu acelaşi număr de atomi de carbon. Există mai multe modalităţi acceptate de denumire a aldehidelor.
Exemplu – Denumirea unor aldehide:
|
CH2 = O |
metanal/formaldehidă/aldehidă formică |
|
CH3 – CH2 – CH = O |
propanal |
|
O = CH – CH = O |
etandial (glioxal) |
Denumirea cetonelor: o metodă de denumire a cetonelor este prin adăugarea sufixului –onă la numele hidrocarburi cu acelaşi număr de atomi de carbon. Există mai multe modalităţi acceptate de denumire a cetonelor.
Exemplu – Denumirea unor cetone:
|
|
propanonă (acetonă) |
|
|
butandionă |
|
|
3-buten-2-onă |
La temperaturi obişnuite, metanalul se găseşte sub formă de gaz, acetaldehida şi acetona sunt lichide, iar celelalte aldehide şi cetone sunt lichide sau solide.
Punctele de topire şi de fierbere ale compuşilor carbonilici cresc cu creşterea masei moleculare. Compuşii carbonilici au puncte de fierbere mai mici decât cele ale alcoolilor cu masă moleculară comparabilă.
Atomul de oxigen din grupa carbonil are două perechi de electroni neparticipanţi datorită cărora aldehidele şi cetonele formează legături de hidrogen cu moleculele de apă. Astfel, compuşii carbonilici cu masă moleculară mică, adică termenii inferiori ai seriei omoloage a compuşilor carbonilici, sunt solubili în apă. Însă, odată cu creşterea masei moleculare, solubilitatea în apă scade. Compuşii carbonilici sunt solubili şi în solvenţi organici, fiind, la rândul lor, buni solvenţi pentru lacuri, vopsele şi chiar unele mase plastice.
Compuşii carbonilici participă la reacţii specifice compuşilor nesaturaţi, şi anume la reacţii de adiţie, oxidare şi polimerizare.
Reacţiile de adiţie ale compuşilor carbonilici decurg după următoarea schemă generală:
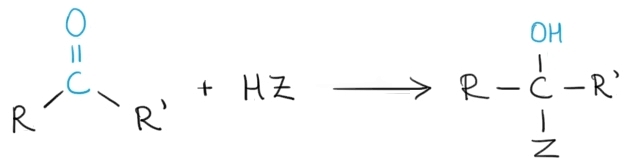
Prin adiţia hidrogenului la aldehide se obţin alcooli primari. Prin adiţia hidrogenului la cetone, se obţin alcooli secundari. Hidrogenarea compuşilor carbonilici se face în prezenţă de catalizatori metalici precum Ni sau Pd.
Reacţiile de oxidare sunt reacţii specifice aldehidelor:
- prin oxidarea aldehidelor cu reactiv Tollens (hidroxid de diaminoargint) se formează acizii carboxilici corespunzători. De exemplu, prin oxidarea aldehidei acetice (CH3 – CH = O) cu reactiv Tollens se obţine acidul acetic şi argint metalic. Argintul metalic se depune pe pereţii vasului formându-se astfel oglinda de argint.
- prin oxidarea aldehidelor cu reactiv Fehling (hidroxid de cupru II) se obţin tot acizii carboxilici corespunzători.