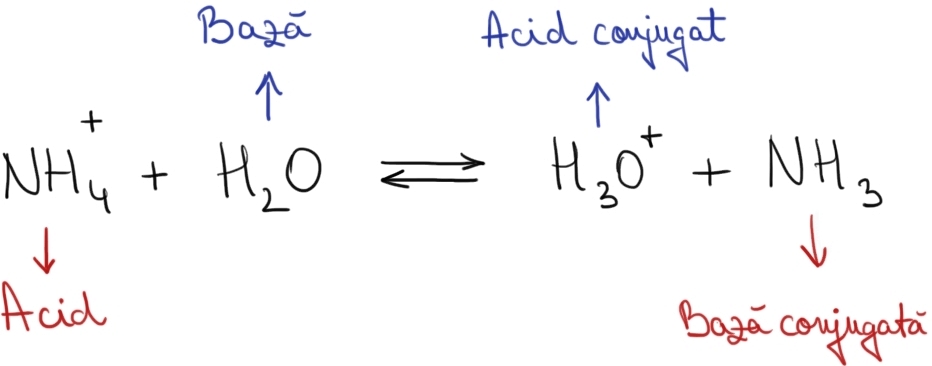Acizi şi baze. Teoria protolitică.
Partajeaza in Google Classroom

Transcript
în primele lecții am discutat despre
cum chimiștii au fost fascinați
Dintotdeauna de periodicitate adică
de proprietățile care se repetă
la elementele din aceeași grupă
am văzut și cam asta a dus la dezvoltarea
chimiei ca știință chimiști sau
oprit doar la studiat periodicitatea
elementelor chimice eu studiat
și proprietățile care se repetă
la compuși chimici ce aparțin unor
anumite categorii două dintre aceste
categorii de compuși care reacționează
împreună respectând un anume model
au fost denumite acizi și baze
toți acizii au anumite proprietăți
comune și la fel și toate bazele
au proprietăți comune chimiștii
au observat că reacția dintre un
acid și o bază anulează atât aciditatea
cât și vaz citația compușilor implicați
așa că au denumit această reacție
reacțiile de neutralizare produșii
reacției de neutralizare sunt în
general o sare și apă dar să vedem
mai întâi Ce sunt acizii și bazele
denumirea de acid vine din limba
latină și înseamnă gust acru înțepător
ca în cazul sucului de lămâie sau
oțetului soluției Ce conține amândouă
acizi să facem totuși o mică paranteza
aici gustul este o caracteristică
extraordinar de periculoasă pentru
acid în multe cazuri să gustăm
un alt și dar putea fi chiar ultimul
lucru pe care îl facem lucru valabil
de altfel și în cazul bazelor de
ce orice ar fi în substanțele chimice
nu se Gustă și nu se inhaleaza
Pe de altă parte compuși din categoria
bazelor a fost denumit inițiali
substanțe alcaline de la cuvântul
arabică alcalii care înseamnă cenușă
pentru că sursa obișnuită pentru
substanțele alcaline era cenușa
de lemn cenușa era încălzită în
amestec cu grăsime animală pentru
a se obține săpunul și se consideră
ei în mod greșit că substanțele
alcaline sunt alunecoase ca săpunul
de fapt aceea era senzația dată
de grăsimile din am este termenul
de alcalin a fost înlocuit de termenul
mult mai general bază terenul de
bază vine de la faptul că un singur
compus adică bază poate fi fundația
de la care se pornește în obținerea
unei serii de săruri diferite prin
reacții cu o selecție de cât vacii
astăzi când vorbim de substanțe
alcaline ne referim doar la bazele
care sunt solubile în apă de exemplu
pornind de la hidroxidul de sodiu
Care este o bază putem obține clorura
de sodiu prin neutralizare cu acid
clorhidric sau pornind de la aceeași
bază putem obține sulfat de sodiu
prin neutralizare cu acid sulfuric
Și totuși Cum identificăm acizii
și bazele fără să Vezi că în viața
Sau în cel mai bun caz fără să
ne alegem cu arsuri grave înainte
să răspundem la această întrebare
la trebui să ne lămurim Ce este
un Proton știu că este o particulă
subatomică din nucleul Atomic însă
în cazul atomului de hidrogen singurul
protoni din nucleu formează însuși
nucleul atomului chimiștii Notează
protonul ca fiind de o ionul de
hidrogen drojin plus adică un atom
de hidrogen care își cedat singurul
electroni din învelișul tonul este
sinonim cu ionul de hidrogen că
este de vreo 2.000 de ori mai greu
decât un electron cu toate astea
un Proton este totuși foarte foarte
ușor și îndeajuns de Sprinter încât
să sară destul de ușor de la omul
ăla alta scăpând din centrul unui
atom de hidrogen protonul Se poate
lipi de norul de electroni al altor
molecule aici poate face rost de
o pereche de electroni puși în
comun și astfel deveni un atom
de hidrogen atașat de molecula
respectivă pe scurt specificul
reacțiilor dintre acizi și baze
constă în transferul protonilor
dar nu se ajunge cât de ușor la
această concluzie chimistul suedezi
vantaa reneos Este cel care a sugerat
că un acid este orice compus care
contine hidrogen și care atunci
când se dizolvă în apă eliberează
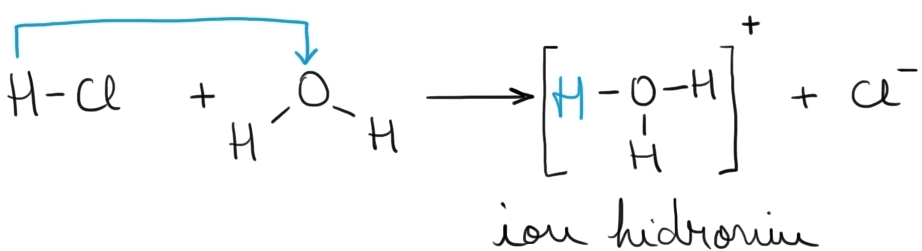
Ion de hidrogen la dizolvarea acidului
clorhidric jos în apă fiecare moleculă
de acid clorhidric cedează un Proton
în soluție nu poate exista liber
deoarece nu are înveliș electronic
astfel el se fixează de o moleculă
de apă și formează ionul hidroniu
în soluție apoasă diluată de acid
clorhidric există numai Ion clorură
și Ion hidroniu des conform lui
arrhenius acid este substanța care
cedează a apei Ion de hidrogen
sau Proton în ceea ce privește
bazele areni o sa spus că o bază
este orice compus a cărui dizolvare
în apă duce la formarea ionilor
hidroxid astfel conform acestei
teorii hidroxidul de sodiu este
o bază deoarece la dizolvarea în
apă Ioni de sodiu și Oxid disociază
complet procesul care are loc la
dizolvarea hidroxidului de sodiu
în apă se poate scrie în această
formă hidroxidul de sodiu plus
un număr n de molecule de apă el
fiind Deci numărul de molecule
de apă care hidratează ionul sodiu
plus chiar la dizolvare se obține
și ionul hidroxi aceste două definiții
ale lui arrhenius țin cont de modelul
reacțiilor de neutralizare observat
de oamenii de știință când o soluție
de acid clorhidric care conform
lui arrhenius conține Ion de hidroniu
și Ion de clorură dizolvat este
turnată peste o soluție de hidroxid
de sodiu care conține Ion de sodiu
și Ion Roxy protonul din componența
ionului hidroniu și ai anul hidroxil
se Grupează imediat și formează
o legătură devenind o moleculă
de apă după ce se formează apa
Ioni de sodiu și clorură formează
sare adică clorura de sodiu ceasta
este reacția de neutralizare însă
prin explicațiile lui arrhenius
nu a acoperit tot ceea ce se întâmplă
cu acizii și bazele teoria lui
avut mult succes pune când te miște
și Au dreptate atenția către reacții
care aveau loc și în alte lichide
în afară de apă sau aveau loc chiar
în absența oricărui solvent adică
oamenii de știință au observat
că mulți compuși se comportă ca
aici sau baze chiar dacă nu este
prezentă apa deși definițiile lui
arrhenius implică în mod explicit
prezența apei în anul 1920 aproape
simultan chimistul englez Thomas
laurii și chimistul Danez Iohannis
bronsted au propus la alte două
definiții mult mai generale pentru
noțiunile de acid și bază luat
în considerare transferul de protoni
care poate avea loc între unele
substanțe sau specii chimice această
teorie asupra acizilor și bazelor
se numește teoria Broșteni Lori
sau se mai numește teoria protolitica
cei doi chimiști au spus foarte
clar și simplu că uneori ce substanță
care poate dona un Proton către
o altă moleculă iar o bază este
orice substanță care poate accepta
acel Proton donate cuvinte una
Ce este un dolar de protoni are
o bază este un acceptor de protoni
conform acestei definiții sunt
acizi și ionul hidroniu Spre exemplu
sau ionul amoniu Ion Luca Taci
la fel conform teoriei protolitice
sunt considerate baze amoniacul
dar și Ioni clorură culpa carbonat
sau eu nu știu fata ce doare ceea
ce știi on pot accepta protoni
trecând în acizi corespunzător
frecvent la Moni o reacție cu apa
va Dona un Proton apei redevenind
amoniac iar apa devine Ion hidroniu
în acest caz ionul amoniu este
acidul acest zi pot dona a mai
mult de un Proton Deci avem și
eu clasificare a lor după numărul
de protoni cedați de o moleculă
minus acizii sunt cei care donează
un singur Proton este cazul acidului
clorhidric acidul uric sau acidului
azotic oly acizii sunt acizii care
pot dauna a doi sau mai mulți protoni
este cazul acidului carbonic sau
acidului sulfuric care sunt Diaz
sau acidul fosforos Care este trioxid
putem spune că polii acizi cedează
protoni în trepte sau mai putem
spune că ionizează în trepte de
exemplu acidul carbonic în reacție
cu apa face da pe un Proton apasă
va transforma în Ion hidroniu iar
acidul carbonic devine Ion carbonat
acid carbonat acid mai poate si
da un Proton unei alte molecule
de apă din soluție și astfel se
transformă în iod carbonat după
cum am mai spus protonul este o
particulă mică extrem de reactivă
iar el nu poate exista liber în
soluție în toate reacțiile despre
care am vorbit protonul cedat de
este acceptat de alta specie chimică
imediat iar conform teoriei protolitice
acea specie care acceptă protonul
este o bază Hai să revenim la reacția
dintre Ion la moneo și apă nu e
foarte clar că reacția dintre ionul
amoniu cel care donează protonul
este acid iar în baza ei este apa
După cum vom vedea în următoarea
lecție când vom vorbi despre Tăria
acizilor eu îl amoniu este un acid
slab și fiind vorba despre un acid
slab are loc și reacția inversă
în reacția inversă observăm că
protonul va fi donat de euro hidroniu
care joacă el acum rol de acid
iar amoniacul va fi cel care acceptă
protonul Deci va fi o bază pentru
de reacție care implică transfer
de protoni fiecare specie chimică
poate fi numită acid sau bază orice
achit prin cedare de protoni se
transformă într o specie chimică
cu caracter de baza si se numește
baza conjugată a acidului respectiv
de ce în acest caz baza conjugată
a ionului de amoniu este amoniacul
la fel orice bază prin faptul că
acceptă un Proton se transformă
între o specie chimică cu caracter
acid adică se transformă într un
acid conjugat al bazei respectiv
iar în acest exemplu apa corespunde
Ion hidroniu ca a citi conjugat
astfel prin teoria protolitica
se stabilește relația achit bază
de tip de noroc chapter prin intermediul
protonului particulă care se transferă
între ei avem de aici cupluri de
acid baza conjugate pe care le
putem reprezenta schematic în acest
fel un acid notat Generic ha1 un
Proton Transformând dusei între
o baza conjugată notată A minus
când bază a minus acceptă un Proton
se transformă la loc în acidul
conjugat a exemple sunt cuplurile
acid baza acid cianhidric și Ionuț
și unora sau acid clorhidric și
Ion îl clorură unde Ionuț și unora
și Ionuț clorură sunt bazele conjugate
și la fel o bază notată b primește
un Proton și se transformă în acidul
conjugat HBO las care la rândul
lui poate dona protonul Transformând
USA la loc în baza b c exemplu
sunt cuplurile acid bază de tipul
Ion amoniu și amoniac unde ionul
amoniu este acidul conjugat al
bazei amoniac am că orice substanță
care poate ceda un Proton este
un acid iar orice substanță care
poate accepta un Proton este o
basm dar știi care este cel mai
des utilizata si in apa și care
este cea mai des utilizată baza
tot apa acest lucru este posibil
datorită caracterului amfoteri
al apei despre care vom discuta
azi data viitoare Și tot atunci
vom discuta și despre Tăria acizilor
și a bazelor