Cromații sunt săruri care conțin ionul cromat, CrO42–, de obicei derivate de la acidul instabil H2CrO4.
Cromații corespund formulei generale M2ICrO4. Ei sunt de culoare galbenă, spre deosebire de dicromați, M2ICr2O7, care sunt de culoare portocalie; se mai cunosc tricromații, M2ICrO10, care sunt de culoare roșie, și tetracromații, M2ICr4O14, care sunt bruni. Cromații alcalini sunt solubili în apă, spre deosebire de cromații de plumb și ai altor metale grele. Soluțiile de cromați și dicromați pot exista într-un echilibru care poate fi deplasat într-un sens sau altul:
2CrO42- + 2H+ 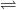 Cr2O72- + H2O
Cr2O72- + H2O
Adăugarea unui acid mărește concentrația ionilor H+ și conduce reacția spre dreapta, de exemplu:
2K2CrO4 + 2HCl = K2Cr2O7 + H2O + 2KCl
Adăugarea unei baze leagă ionii H+ și conduce reacția spre stânga, de exemplu:
K2Cr2O7 + 2KOH = 2K2CrO4 + H2O
În industrie, ca materie primă pentru prepararea cromaților se folosește cromitul. Acesta se calcinează cu un amestec de var și carbonat de sodiu, la 1100-1300°C:
4(Cr2O3·FeO) + 7O2 + 8Na2CO3 = 8Na2CrO4 + 2Fe2O3 + 8CO2
Varul adăugat servește pentru realizarea porozității produsului ce trebuie supus calcinării.
Prin tratarea dicromaților cu un carbonat alcalin se obțin cromații respectivi:
Na2Cr2O7 + Na2CO3 = 2Na2CrO4 + CO2
Dicromații în soluții acide fiind agenți de oxidare puternici pot oxida, de exemplu, sulful din acidul sulfuros:
K2Cr2O7 + 3H2SO3 + H2SO4 = K2SO4 + Cr2(SO4)3 + 4H2O
sau iodul din iodura de potasiu:
K2Cr2O7 + 7H2SO4 + 6KI = Cr2(SO4)3 + 3I2 + 4K2SO4 + 7H2O
Cromații în soluție bazică sunt agenți de oxidare mai slabi.
În reacțiile de oxidare a diferitelor substanțe, cromul de la numărul de oxidare +6 este redus la numărul de oxidare +3.
Prin tratarea soluțiilor unui cromat sau dicromat alcalin cu soluțiile unor săruri de metale grele se obțin de multe ori precipitate colorate. Astfel, cu o soluție de clorură de bariu se formează un precipitat galben de cromat de bariu:
K2CrO4 + BaCl2 = BaCrO4 + 2KCl
Cu o soluție de azotat de plumb se formează un precipitat galben de cromat de plumb:
K2CrO4 + Pb(NO3)2 = PbCrO4 + 2KNO3
Cu o soluție de azotat de argint se formează un precipitat roșu închis de cromat de argint:
K2CrO4 + 2AgNO3 = Ag2CrO4 + 2KNO3
Cromații metalelor grele sunt utilizați ca pigmenți de crom. Astfel, galbenul de crom este cromatul neutru de plumb, PbCrO4; roșul de crom este un cromat bazic de plumb, PbCrO4·Pb(OH)2; portocaliul de crom este un amestec de cromat neutru și cromat bazic de plumb; galbenul de zinc este o sare dublă de cromat de zinc și dicromat de potasiu, 3ZnCrO4·K2Cr2O7. Pigmenții de crom sunt rezistenți la aer și umiditate și au o bună putere de acoperire. Sunt însă toxici.
Dicromații se utilizează în tăbăcirea rapidă cu crom, ca oxidanți în chimia organică, în pirotehnie (ca înlocuitori ai cloratului de potasiu), la înălbirea uleiurilor și cerurilor, la prepararea gelatinei cu crom pentru zincografie (după iradiere cu lumină această gelatină devine impermeabilă față de apă) etc.






