Atomul
Chimia este ştiinţa care se ocupă cu studiul materiei şi a transformărilor pe care materia le suferă.
Materia este orice lucru care are grutate şi ocupă spaţiu; este peste tot în jurul nostru. Materia este formată din substanţe care la rândul lor conţin molecule, ioni sau atomi.
Substanţele sunt de două feluri:
- substanţe simple (conţin molecule formate din atomi identici): O2, H2
- substanţe compuse (conţin molecule formate din atomi diferiţi): H2O, CuSO4
Atomul (din greacă: indivizibil) este cea mai mica particulă posibilă care încă mai păstrează proprietăţile unei substanţe. Atomii au proprietăţi fizice şi chimice specifice în funcţie de numărul şi aranjamentul celor trei particule subatomice:
- electroni: e-
- protoni: p+
- neutroni:
Structura atomului: atomul este format dintr-un nucleu care conţine protoni şi neutroni, şi un înveliş electronic care este o zonă difuză în jurul nucleului unde se găsesc electronii.

Proprietăţile particulelor subatomice:
|
Numele particulei
|
Simbol
|
Masă (kg) (u. a. m.)
|
Sarcină electrică
|
|
Electron
|
e-
|
9.1093 x 10-31 0.000548
|
-1
|
|
Proton
|
p+
|
1.6727 x 10-27 1.007277
|
+1
|
|
Neutron
|
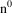
|
1.6749 x 10-27 1.008665
|
0
|
Numărul atomic se notează cu Z şi reprezintă numărul de protoni din nucleul unui atom. Prin numărul atomic, un atom se diferenţiază de ceilalţi atomi. Z reprezintă şi numărul de ordine al unui atom în tabelul periodic, cât şi numărul de electroni în cazul atomilor neutri.
Sarcina nucleară a unui atom este pozitivă şi egală cu numărul de protoni din nucleu; se notează cu simbolul +Z. În cazul atomilor neutri, numărul protonilor este egal cu numărul electronilor din învelişul electronic. Sarcina nucleară pozitivă este anulată de sarcina electronica negativă.
Atomii care au acelaşi număr atomic Z şi aceeaşi sarcină nucleară +Z formează un element chimic.
Numărul de masă al unui atom se notează cu A şi reprezintă suma dintre numărul de protoni şi numărul de neutroni din nucleul unui atom.
A = Z + N, unde N este numărul de neutroni
Aşadar, mărimile care caracterizează un element chimic sunt numărul atomic Z şi numărul de masă A. Acestea se scriu în faţa simbolului elementului chimic după cum este reprezentat în imaginea de mai jos:

Exemplu:
Atomul de carbon are simbolul 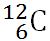 . Astfel deducem că atomul de carbon are următoarele particule subatomice:
. Astfel deducem că atomul de carbon are următoarele particule subatomice:
- 6 p+
- 6 e-
- 12 – 6 = 6
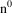

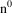

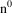

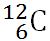 . Astfel deducem că atomul de carbon are următoarele particule subatomice:
. Astfel deducem că atomul de carbon are următoarele particule subatomice:




