Cromul, Cr, este un metal de tranziție alb-argintiu, foarte dur din grupa 6 a tabelului periodic (grupa a VI-a secundară sau grupa VI B); are numărul atomic 24 și masa atomică 52,00. Punctul de topire al cromului este 1857°C, iar punctul de fierbere este 2672°C. Minereul principal din care se extrage cromul este cromitul, FeO·Cr2O3.
Cromul se găsește răspândit în natură sub formă de combinații, mai ales sub formă de cromit, FeO·Cr2O3, și de crocoiză, PbCrO4. De multe ori cromul însoțește aluminiul în minereurile acestuia.
Cromul pur se obține din oxid de crom prin aluminotermie:
Cr2O3 + 2Al = 2Cr + Al2O3; 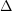 H = - 130 kcal/mol
H = - 130 kcal/mol
De obicei, în tehnică se folosește ca materie primă cromitul, deoarece nu se urmărește obținerea metalului pur, ci a aliajului său cu fierul, ferocromul. În acest scop, cromitul se reduce cu cărbune, în cuptoare electrice:
FeO·Cr2O3 + 4C = Fe + 2Cr + 4CO
Cromul este un metal alb-argintiu, foarte dur, însă fărâmicios; are un puncte de topire și de fierbere foarte ridicate, 1857°C, respectiv 2672°C. Se poate lustrui bine obținându-se o suprafață argintie foarte strălucitoare. În stare compactă este de o deosebită rezistență la agenții atmosferici și la oxidare, chiar și la temperaturi mai ridicate. Nu arde în oxigen decât la temperaturi peste 2000°C. La temperaturi înalte cromul se combină direct cu halogenii, sulful, azotul, carbonul, siliciul și cu unele metale. Cromul este atacat de acidul clorhidric sau de acidul sulfuric diluat. Față de acidul azotic și apa regală cromul devine pasiv din cauza formării unui strat de oxid insolubil în acizi.
Din cauza poziției lui în seria tensiunilor electrochimice, cromul poate înlocui multe metale din soluțiile sărurilor lor, de exemplu cuprul, staniul, nichelul. Tot din această cauză poate descărca ioni de hidrogen, de unde rezultă activitatea lui față de acizi. În stare pasivă însă, cromul este mult deplasat spre dreapta în seria tensiunilor, astfel încât se comportă ca un metal nobil.
În stare fin divizată, cromul este mult mai activ; se aprinde cu ușurință în aer și este atacat puternic de acizi.
Cromul se întrebuințează pentru acoperirea altor metale cu un strat fin de crom, făcându-le rezistente față de agenții atmosferici și chimici și în același timp atrăgătoare ca aspect. Depunerea stratului de crom peste alte metale se face prin electroliză și poartă numele de cromaj sau cromare.
Cel mai mult este întrebuințat cromul pentru obținerea unor oțeluri speciale caracterizate prin mare rezistență și duritate, folosite pentru construirea ustensilelor sau pieselor de mașini foarte solicitate, de exemplu bile pentru rulmenți. La fabricarea oțelurilor speciale - inoxidabile - nu se adaugă crom pur, ci ferocrom, cu 50-70% Cr și un procent cât mai mic de carbon.
Uneori, în compoziția oțelurilor cu crom se mai adaugă și un al treilea metal, de exemplu nichel, wolfram sau molibden. Asemenea oțeluri ternare sunt rezistente la coroziune; de aceea se folosesc la construcția de aparate și rezervoare în industria chimică.
În industria electrochimică se folosesc rezistențe electrice pentru cuptoare - făcute dintr-un aliaj de Fe-Ni-Cr, numit nichel-crom (sau nicrom).
În combinațiile sale, cromul poate manifesta mai multe numere de oxidare:
Combinațiile cromului
Număr de
oxidare |
Oxizi
Formulă |
Oxizi
Caracter |
Hidroxizi
Formulă |
Ioni în soluție
Formulă |
Ioni în soluție
Culoare |
| +2 |
CrO |
bazic |
- |
Cr2+ |
albastru |
| +3 |
Cr2O3 |
amfoter |
Cr2O3·xH2O |
Cr3+
[CrO2]- |
verde sau
violet |
| +6 |
CrO3 |
acid |
H2CrO4 |
[CrO4]2- |
galben |
Numărul de oxidare maxim +6 corespunde poziției elementului în tabelul periodic. Numerele de oxidare +2 și +3 sunt datorate participării unuia sau a doi electroni din nivelul 3d, în afara electronului 4s1. În puține cazuri, cromul poate forma combinații în care manifestă numerele de oxidare +5 și +4; foarte rar poate avea numărul de oxidare +1.
Cromul(VI), care există numai în specii ca CrO
3, CrO
42- și CrO
2F
2, este puternic oxidant. Cu elemente din
grupa 16 (grupa VI A), cromul se aseamănă prin aciditatea trioxidului. Starea cea mai stabilă și importantă este Cr(III).
Combinațiile cromului(II) se obțin prin reducerea combinațiilor cromului(III), de exemplu cu zinc în soluție acidă:
Cr3+ + 1/2 H2 = Cr2+ + H+
sau prin oxidarea cromului metalic, de exemplu, prin tratare cu acizi:
Cr + 2H+ = Cr2+ + H2
Soluțiile combinațiilor de crom(II) sunt colorate în albastru-azur; sărurile anhidre de crom(II) au alte culori.
Combinațiile cromului(II) prezintă asemănări cu combinațiile elementelor de tranziție vecine: mangan(II), fier(II), cobalt(V), nichel(II). Ele sunt însă mai puțin stabile și mai puternic reducătoare. Astfel, în contact cu aerul trec imediat în combinații ale cromului(III). Această trecere are loc chiar în soluții apoase.
Pentru puterea lor reducătoare sunt folosite în industria coloranților.
Combinațiile cromului(III) derivă de la
oxidul cromic, Cr
2O
3, care are caracter amfoter. Ele manifestă tendința accentuată să formeze complecși, din care cauză de multe ori în soluții nu dau reacțiile caracteristice ionilor Cr
3+. Acești ioni, în soluții diluate, se găsesc sub formă hidratată. Din moleculele de apă legate în ionul complex, șase molecule sunt mai strâns legate de ionul central și de aceea sărurile care cristalizează din soluție au compoziția [Cr(H
2O)
6]X
3. Aceste săruri sunt colorate violet.
Sărurile ionului Cr
3+ hidratate au multe asemănări cu sărurile aluminiului: formează
alauni, hidrolizează în soluție apoasă, tind să formeze complecși în care au numărul de coordinație șase, etc. Cauza acestei asemănări este valența identică, precum și dimensiunea foarte apropiată a razei ionice (la Cr
3+ = 0,65 Å; la Al
3+ = 0,57 Å).
Sărurile cromului(III) în soluție alcalină pot fi oxidate cu ușurință de către clor, brom, hipocloriți, apă oxigenată etc., formând
cromați. Astfel, dacă o soluție de sulfat de crom alcalinizează cu o soluție de hidroxid de sodiu în exces (până la dispariția precipitatului de hidroxid cromic), se tratează cu o cantitate mică de apă de brom, soluția devine galbenă din cauza formării
cromatului de sodiu:
Cr2(SO4)3 + 16NaOH + 3Br2 = 2Na2CrO4 + 6NaBr + 3Na2SO4 + 8H2O
Combinațiile cromului(VI) derivă de la
trioxidul de crom, CrO
3, care este o anhidridă acidă.
Acizii cromici nu s-au putut separa încă; ei se cunosc numai în soluție apoasă. Sărurile lor se cunosc însă în stare liberă.
Cromații sunt săruri care conțin ionul cromat, CrO
42-, și reprezintă o categorie diversă și importantă a combinațiilor de crom(IV).
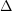 H = - 130 kcal/mol
H = - 130 kcal/mol





