Influenţa catalizatorilor asupra vitezei de reacţie
Tag-uri
Partajeaza in Google Classroom
Teorie: Teorie - Influenţa catalizatorilor asupra vitezei de reacţie Descarcă PDF
Catalizatorul este o substanţă ce participă la o reacţie chimică şi măreşte viteza acestei reacţii. Catalizatorii nu influenţează în niciun alt fel reacţia şi produşii care se obţin. De asemenea, catalizatorii nu suferă nicio schimbare chimică netă în timpul reacţiei. Aşadar, catalizatorii nu se consumă, ei pot fi reciclaţi.
Reacţiile catalitice sunt reacţiile care au loc în prezenţa catalizatorilor.
Modul de funcţionare al catalizatorilor: catalizatorii oferă un mecanism de reacţie alternativ ce presupune o stare de tranziţie diferită şi o energie de activare mai scăzută. Reacţia catalitică va decurge în mai multe etape, şi fiecare etapă a reacţiei se caracterizează printr-o energie de activare mai mică decât energia de activare a reacţiei necatalizate. Iar totalul energiilor de activare al etapelor reacţiei catalizate este mai mic decât energia de activare a reacţiei necatalizate.
Exemplu – Pentru o reacţie catalitică ce are loc în trei etape:
Ea1 + Ea2 + Ea3 < Ea - reacţie necatalizată , unde Ea1, Ea2, Ea3 sunt energiile de activare ale celor 3 etape ale reacţiei catalitice.
Etapa lentă a unei reacţii catalitice care decurge în mai multe etape este etapa determinantă de viteză. Etapa lentă este cea care necesită energia de activare cea mai ridicată dintre toate etapele de reacţie, astfel că viteza reacţiei catalitice coincide cu viteza etapei lente.
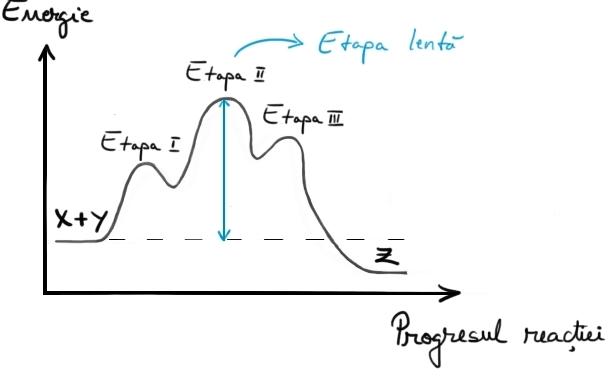
Diagrama energetică pentru o reacţie catalitică ce are loc în trei etape; în acest caz, etapa a doua este etapa determinantă de viteză.
Printre cele mai importante proprietăţi ale catalizatorilor se numără activitatea catalitică şi selectivitatea.
Activitatea catalitică se măsoară prin numărul de molecule de reactant care se transformă în unitatea de timp, pe unitatea de suprafaţă de catalizator. Catalizatorii sunt preparaţi în aşa fel încât suprafaţa de contact cu reactanţii să fie cât mai mare. Activitatea catalitică scade în timp şi este influenţată de promotori şi otrăvuri.
Promotorii sunt substanţe care îmbunătăţesc proprietăţile catalitice, de exemplu, mărind activitatea catalitică a catalizatorilor. Promotorii nu pot modifica viteza de reacţie în absenţa catalizatorilor.
Otrăvurile sunt substanţe care diminuează sau chiar anulează activitatea catalitică.
Inhibitorii sunt substanţe care au capacitatea de a micşora viteza reacţiilor chimice, acţionând asupra reactanţilor.
Selectivitatea reprezintă capacitatea unui catalizator de a favoriza o anumită reacţie, din mai multe posibile; este capacitatea de a dirija transformarea chimică, preferenţial, spre formarea unui anume produs de reacţie acolo unde s-ar fi putut forma mai mulţi produşi.
Tipuri de reacţii catalitice:
Reacţiile catalitice omogene sunt reacţiile în care reactanţii şi catalizatorul formează o singură fază, de cele mai multe ori, faza lichidă.
Substanţe care, în mediu lichid, pot acţiona drept catalizatori omogeni sunt următoarele: acizi, baze, ioni hidroxil, ioni hidroniu, combinaţii complexe ale metalelor tranziţionale.
Reacţiile catalitice eterogene sunt reacţiile în care reactanţii şi catalizatorul nu aparţin aceleiaşi faze – reacţia chimică are loc la interfaţa formată de fazele aflate în contact. Aşadar, în cataliza eterogenă sunt posibile tot felul de combinaţii de stări de agregare ale catalizatorilor şi ale reactanţilor. Însă, cel mai mare interes practic îl prezintă reacţia amestecurilor de gaze sau lichide pe catalizatori solizi.
În general, în cataliza eterogenă, catalizatorii au nevoie de un suport solid pe care să fie depuşi, numit suport catalitic. Suportul catalitic poate îmbunătăţi calităţile mecanice ale catalizatorului şi este, de obicei, un material solid, poros.
Drept suport catalitic se pot utiliza materiale precum argile, azbest, cărbune activ, piatră ponce şi oxid de aluminiu.
Reacţiile catalitice enzimatice sunt reacţiile în care catalizatorul este o enzimă. Enzimele sunt proteine extrem de importante de care depind toate organismele vii pentru ca procesele biochimice să aibă loc în timp util. Există şi multe procese industriale în care se folosesc enzimele drept catalizatori.






