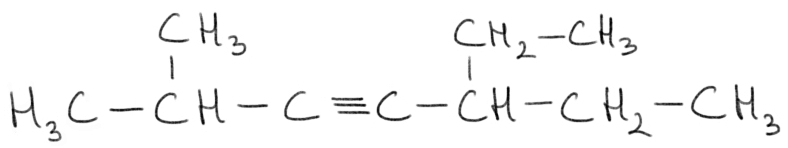Alchine – nomenclatură, proprietăţi fizice
Partajeaza in Google Classroom

Transcript
a văzut că alchenele sunt hidrocarburi
nesaturate care conțin o legătură
dacă mai adăugăm o legătură Pi
la legătura dublă obținem o nouă
clase de compuși organici cu un
grad de nesaturare și mai mare
decât al Chinei și anume alchinele
Deci avem până acum alcani alchene
alchine denumirile acestora carburi
sunt foarte asemănătoare să facem
o scurtă recapitulare alcanii au
în molecula lor numai legături
simple între atomii de carbon alchenele
prezintă și o legătură dublă între
doi dintre atomii de carbon din
molecula iar sinele prezintă o
legătură triplă alcanii sunt hidrocarburi
saturate atomi de carbon formează
legături cu alți patrulaterele
și alchinele sunt hidrocarburi
rate atomi de carbon participanți
la legătura dublă formează legături
cu alți trei atomi iar atomi de
carbon participanți la legătura
triplă formează legături cu alți
doi Așadar alchinele sunt hidrocarburi
nesaturate care conțin în molecula
lor o legătură între doi atomi
de carbon albinele au Catena aciclică
liniară sau ramificată formula
lor generale este galben n hidrogen
2 n-2 observăm că Pe măsură ce
crește gradul de nesaturare avem
tot mai puțini atomi moleculele
hidrocarburilor dacă locuim pe
an din această formulă generală
cu valori întregi și succesiv începând
cu 2 obținem seria omoloaga alchinelor
Haideți împreună câteva alicele
primul termen al seriilor de alchene
ilor conține doi atomi de carbon
Deci prefixul corespunzător este
et la care adăugăm sufixul specific
alchinelor adică in decea descompusă
numește etena denumirea uzuală
este acetilenă după această denumire
albinele se mai numesc și acele
următorul termen are trei atomi
de carbon Deci se numește propena
începând cu cel de al treilea termen
al serii omul lua c precizăm și
poziția legăturii triple în denumire
alchene în continuare avem patru
atomi de carbon Deci prefixul este
bat iar legătura tripla se află
imediat după Primul atom de carbon
asta înseamnă că se află poziția
1 Deci denumirea compusului este
1-butina următoarea China are tot
patru atomi de carbon dar legătura
triplă se află după cel de al doilea
atomi de carbon de sarcină se numește
2-butina în cazul catenelor mai
mari numerotam Catena astfel încât
rigla legătură să aibă indicele
de poziție cel mai mic posibil
din acest punct de vedere al poziției
legături triple alchinele pot avea
legătura triplă la capătul ca tine
iar atunci sunt albine marginale
deci 1-butina este o alchenă marginală
sau atunci când au legătura triplă
în interiorul catenei alchinele
se mai numesc al Chinei interne
deci 2-butina este o alchenă internă
1-butina și 2-butina sunt izomeri
de poziție Așadar vedem că alchinele
cu mai mult de 3 atomi de carbon
în molecula prezintă izomerie de
poziție radicalii monovalenti ai
alchinelor adică radicali alchil
se denumesc prin înlocuirea sufixului
Inna al Chinei cu sufixul de exemplu
acesta este radicalul retinil iar
acesta este radicalul 2 proprii
care se mai numește și propargil
în cazul acțiunilor atomi de carbon
implicați în legătura triplă se
numesc atomi de carbon Miti nici
iar atomii de Carboni vecini adică
ce adiacenți celor implicați legătura
triplă se numesc atomi de carbon
propargilic inele cu catenă ramificată
se numesc izvoare Izvoarele se
denumesc asemănător cu Izvoarele
alegem cea mai lungă Catena care
conține legătura tripla avem grijă
ca indicele de poziție a legăturii
triple să aibă valoarea cea mai
mică în cazul acestei molecule
avem cu verde numerotarea corectă
iar în cazul în care avem substituenți
îi vom denumi în ordine alfabetică
la al doilea atom de carbon avem
o radicali metil iar la atomul
de carbon cu numărul 5 avem un
radical Eti legătura triplă se
află în poziția cu numărul 3 Așadar
compusul nostru se numește Open
2 ml3 haptena dacă am fi numerota
greșit Catena ar fi obținut o denumire
incorectă și anume 3 din 6 m 4
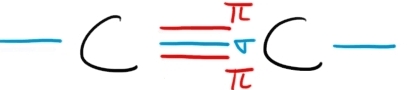
haptena legătura triplet este formată
din troll legături Sigma și două
legături pi de carbon care formează
această legătură triplă sunt vizați
expresia mintim că fiecare atomizat
spre are doi orbitali hibridizat
și doar vitel de tip divizați când
se formează legătura triplă fiecare
atom de carbon participă la formarea
legăturii cu câte un orbital de
tip este mai participă la legătura
triplă și cu câte doi orbitali
de tip p prin întrepătrunderea
orbitalilor de tip s p se formează
o legătură Sigma prin interacțiunea
dintre orbitali de tip p se formează
două legături pi Aceasta este o
legătură Pi iar aceasta este a
doua legătură Pi mai adăugăm și
câte un orbital s de la doi atomi
de hidrogen și am obținut acetilena
sau etena prezența acestor două
legături pi face ca legătura triplă
Din acetilenă și din alte nele
marginale să fie polară Polul pozitiv
se află la atomul de hidrogen iar
Polul negativ la atomul de carbon
triplu legat în consecință aceștia
atomi de hidrogen legat de atomi
de Carboni implicați într o legătură
triplă au un caracter slabă țin
asta face ca am alchinele să fie
parțial solubile în apă spre diferență
de alcani alchene care sunt insolubile
în apă planurile în care se găsesc
cele două legături pi sunt perpendiculare
între ele și sunt perpendiculare
Și Pe planul în care se găsește
legătura ce lucru o face imposibilă
rotația liberă în jurul legături
triple pentru că atomi de carbon
implicați în legătura triplă mai
sunt legați Numai decât un singur
alta tocănel a nu prezintă izomerie
geometrică așa cum se întâmplă
în cazul acelor alchinele pot prezenta
numai izomeri de constituție după
cum am zis mai devreme alchinele
cu mai mult de 3 atomi de carbon
prezintă izomerie de pozitie în
cazul izomerilor de poziție diferă
poziția la care se află legătura
tripla așa cum este cazul 1-butenei
și a2 putine albinele care au mai
mult de trei atomi de carbon prezintă
și izomeri de catenă este cazul
acestor domnule cool a 1 pentena
și 3 m nu buton izomeria de poziție
și izomeria de catenă sunt subcategorii
ale izomeriei de constituție Acum
am văzut și mai devreme atomi de
carbon hibridizat SP cel mai atrăgător
de electroni decât atomii de carbon
hibridizat sp3 sau sp2 de cine
legăturile simple carbon carbon
și legăturile simple carbon hidrogen
vecini legături triple sunt la
bal are aer asta face ca interacțiunile
dintre moleculele de alchene să
fie mai puternice pe lângă forțele
intermoleculare Vanderbilt sunt
prezente și forte de dispersie
depo Depot ca și consecință deși
alchinele au mase moleculare mai
mici decât Aleea lichidelor sau
alcanilor cu același de atomi de
carbon punctele de fierbere a lichidelor
sunt mai ridicate la fel se întâmplă
și în cazul densității densitatea
lichidelor e mai mare decât densitatea
alcanilor sau alchenelor corespunzătoare
dar e mai mică decât densitatea
primii trei termeni ai seriei până
la 1:00 butina sunt gaze începând
cu 2-butina alchinele sunt mici
iar termenii superior sunt solid
hainele sunt solubile în solvenți
organici iar datorită caracterului
slaba si dai la Tomi lor de hidrogen
din jurul legături triple alchinele
sunt parțial solubile și în apă
se dizolvă în drum volum de apă
la temperaturi și presiuni obișnuite
iar solubilitatea crește cu creșterea
presiunii