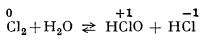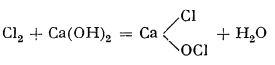Acidul hipocloros, HClO, este un oxoacid al clorului în care atomul de clor are numărul de oxidare +1. Acidul hipocloros este un acid lichid stabil numai în soluție; este un acid foarte slab, dar este un oxidant blând și e foarte folosit ca agent de albire.
Preparare
Acidul hipocloros se obține odată cu acidul clorhidric prin acțiunea clorului asupra apei (formarea apei de clor). Are loc un proces de oxido-reducere (disproprorționare), deoarece clorul, când trece în acid clorhidric, își schimbă numărul de oxidare de la zero la -1, iar când trece în acid hipocloros își schimbă numărul de oxidare de la zero la +1:
Din cauza acizilor formați, soluția are un caracter slab acid; culoarea ei galbenă și mirosul caracteristic, indică, însă, și prezența clorului liber, dovedind prin aceasta că reacția este reversibilă.
Pentru ca soluția să nu mai conțină clor liber, echilibrul reacției trebuie deplasat spre dreapta. Aceasta se poate realiza prin adăugarea, fie a unei substanțe oxidabile (care să lege oxigenul rezultat prin descompunerea acidului hipocloros: HClO → HCl + O), fie prin adăugarea unei baze (care să formeze cu cei doi acizi sărurile respective).
Pentru ca soluția să conțină însă clor liber, echilibrul reacției trebuie deplasat spre stânga, ceea ce se poate realiza prin adăugarea de acid clorhidric.
Acidul hipocloros este foarte instabil; se descompune sub acțiunea luminii sau căldurii în acid clorhidric și oxigen. Din această cauză are mare putere oxidantă și decolorantă; decolorează turnesolul și indigoul, pune în libertate iodul din ioduri și oxidează sărurile de mangan, plumb, etc. la săruri cu grad superior de oxidare.
Cl2 + 2HO- → ClO- + Cl- + H2O
Ei se caracterizează printr-o mare putere oxidantă, din care cauză se folosesc drept decoloranți. Cei mai importanți sunt hipocloritul de sodiu și hipocloritul de potasiu. Aceștia fiind instabili, se obțin numai sub formă de soluții.
Clorura de var nu este o substanță unitară, ci un amestec de diferite săruri de calciu obținute prin trecerea unui curent de clor peste hidroxid de calciu uscat; componentul principal al clorurii de var este o sare mixtă a acidului hipocloros și acidului clorhidric:
Aceasta este o pulbere albă cu miros de clor, care în aer umed este descompusă de bioxidul de carbon, cu punerea în libertate a acidului hipocloros. De aceea, clorura de var are o acțiune puternic oxidantă. Prin încălzire se descompune cu degajare de oxigen:
2CaOCl2 → 2CaCl2 + O2
Prin tratare cu acid clorhidric pune clor în libertate:
CaOCl2 + 2HCl → CaCl2 + H2O + Cl2
Cantitatea de clor degajată la tratare cu acid clorhidric (“clor activ”) este un criteriu de apreciere a calității clorurii de var. Clorura de var se întrebuințează ca decolorant pentru bumbac, hârtie, celuloză, ca dezinfectant ieftin pentru apele reziduale, ca insecticid, la clorurarea unor substanțe organice, ca dezinfectant contra iperitei, etc.